A ACESSE tem como principal objetivo o fomento do ecossistema de pesquisas clínicas no Brasil, sendo a logística no processo de amostras biológicas em estudos multicêntricos um tema especialmente sensível para a segurança de pacientes e para a competitividade do país.
A necessidade de envio de amostras biológicas para o exterior requer logística complexa com diversos pontos de estrangulamento e potencias falhas que impactam o bom andamento dos projetos, sendo os principais problemas o atraso na liberação dos resultados, instabilidade das amostras e perda de exames (não recebimento) pelo laboratório central.
Assim, o papel dos laboratórios centrais nos estudos clínicos é essencial para assegurar a qualidade, a confiabilidade e a rastreabilidade dos dados gerados. A integridade dos resultados laboratoriais impacta diretamente na segurança dos participantes e na validade científica do estudo. Qualquer falha de compliance — seja no envio tardio dos resultados, seja em problemas de transporte que comprometam a integridade das amostras — pode gerar riscos éticos e clínicos significativos.
1. Impactos Éticos e de Segurança
Atrasos na liberação de resultados laboratoriais podem comprometer o acompanhamento clínico dos participantes, retardando decisões médicas críticas e expondo-os a riscos evitáveis. Da mesma forma, a corrupção de amostras por falhas no transporte ou armazenamento compromete a validade dos dados e pode levar a interpretações equivocadas sobre a segurança ou eficácia do produto em investigação.
Essas situações violam princípios bioéticos fundamentais, como:
- Beneficência e não maleficência: garantir que os participantes recebam o máximo benefício possível e não sejam expostos a danos evitáveis. O processo de recoleta de amostras biológicas por problemas logísticos não pode ser entendido como algo simples ou sem consequências maiores. Trata-se de processo invasivo, que gera dor e incômodo, além de interferir diretamente no engajamento do participante.
- Justiça: assegurar que todos os participantes tenham acompanhamento adequado e equitativo. Os atrasos em resultados por vezes prejudicam o bom acompanhamento clínico.
- Ainda, no processo de centralidade do paciente, com absoluta certeza as falhas logísticas que necessitam de frequentes recoletas de amostras não contribui positivamente para a experiência do participante.
- Outro aspecto significativo é o maior numero de amostras canceladas em centros de pesquisa fora de capitais e com menos opções logísticas e malhas aéreas. Isso acaba por dificultar e atrasar a inclusão de pacientes por esses centros, afetando o processo adequado de diversidade, tão relevante para a pesquisa clínica.
- 2. Responsabilidade dos Laboratórios Centrais e Capacidade do Brasil para atuação com Laboratórios Centrais
- Os processos laboratoriais também devem ser objeto de monitoramento e auditoria. Assim, os laboratórios centrais devem adotar Procedimentos Operacionais Padrão (POPs) claros e revisados regularmente, assegurando:
- Cadeia de custódia rigorosa para transporte e armazenamento de amostras.
- Sistemas de monitoramento de temperatura e rastreabilidade logística.
- Prazos definidos e cumpridos para emissão de resultados.
- Comunicação imediata de desvios ou falhas ao patrocinador e ao investigador principal.
- O não cumprimento dessas práticas configura não apenas uma falha operacional, mas também uma violação ética, pois coloca em risco a segurança dos participantes e a credibilidade científica do estudo.
- O Brasil possui laboratórios de excelência que podem ser utilizados como laboratórios centrais , minimizando os riscos de corrupção de amostras devidos aos processos longos de transporte.
- Justiça: assegurar que todos os participantes tenham acompanhamento adequado e equitativo. Os atrasos em resultados por vezes prejudicam o bom acompanhamento clínico.
- Autonomia: respeitar o direito dos voluntários de participar de um estudo que lhes ofereça condições seguras e transparentes. As repetidas recoletas de amostras por falha nos processos de logística não está usualmente indicada em TCLE.
Ainda, no processo de centralidade do paciente, com absoluta certeza as falhas logísticas que necessitam de frequentes recoletas de amostras não contribui positivamente para a experiência do participante.
Outro aspecto significativo é o maior numero de amostras canceladas em centros de pesquisa fora de capitais e com menos opções logísticas e malhas aéreas. Isso acaba por dificultar e atrasar a inclusão de pacientes por esses centros, afetando o processo adequado de diversidade, tão relevante para a pesquisa clínica.
2. Responsabilidade dos Laboratórios Centrais e Capacidade do Brasil para atuação com Laboratórios Centrais
Os processos laboratoriais também devem ser objeto de monitoramento e auditoria. Assim, os laboratórios centrais devem adotar Procedimentos Operacionais Padrão (POPs) claros e revisados regularmente, assegurando:
- Cadeia de custódia rigorosa para transporte e armazenamento de amostras.
- Sistemas de monitoramento de temperatura e rastreabilidade logística.
- Prazos definidos e cumpridos para emissão de resultados.
- Comunicação imediata de desvios ou falhas ao patrocinador e ao investigador principal.
O não cumprimento dessas práticas configura não apenas uma falha operacional, mas também uma violação ética, pois coloca em risco a segurança dos participantes e a credibilidade científica do estudo.
O Brasil possui laboratórios de excelência que podem ser utilizados como laboratórios centrais , minimizando os riscos de corrupção de amostras devidos aos processos longos de transporte.
1. Logística de Recebimento de Kits e seus Impactos Diretos
A necessidade de importação de kits de coleta não encontra justificativa, visto absolutamente todos os materiais e reagentes estarem disponíveis nos país. É frequente o atraso no recebimento, assim como limitação da quantidade de kits, o que pode limitar gravemente o nível de recrutamento dos centros de pesquisa.
3. Impactos na Avaliação dos Centros e na Qualidade Científica dos Estudos
Repetidos erros ou falhas no processamento e transporte de amostras, bem como atrasos na entrega de resultados laboratoriais, não afetam apenas a segurança e o seguimento clínico dos participantes. Esses problemas repercutem diretamente na forma como o centro de pesquisa é percebido pelos patrocinadores. Ainda que a responsabilidade primária seja do laboratório central, a cobrança inicial recai sempre no centro de pesquisa (frequentemente questionado em seus processos, independente da experiencia ou comprovação de robustez e qualidade nos mesmos). Isto pode comprometer sua reputação e reduzir suas chances de ser selecionado para futuros projetos clínicos.
Além disso, inconsistências nos resultados laboratoriais impactam negativamente a qualidade científica do estudo. Dados corrompidos ou atrasados prejudicam as análises estatísticas, comprometem endpoints críticos e podem levar a conclusões equivocadas sobre a segurança ou eficácia do produto investigacional. Esse cenário não apenas fragiliza a validade do estudo, mas também coloca em risco o compromisso ético de oferecer aos participantes uma pesquisa conduzida com rigor e responsabilidade.
Outro ponto a ser considerado é o processo complexo de agendamentos de envio de amostras laboratoriais para o exterior. Os processos são trabalhosos e requerem equipe dedicada para o agendamento e preparo de documentação. A opção de laboratórios centrais no Brasil não apenas diminuiriam os problemas previamente indicados, mas também reduziria de forma importante os custos dos centros no processo burocrático de agendamento e preparação de embarques para o exterior.
Os gráficos a seguir mostram as demandas de um centro de pesquisa com mais de 20 projetos ativos:
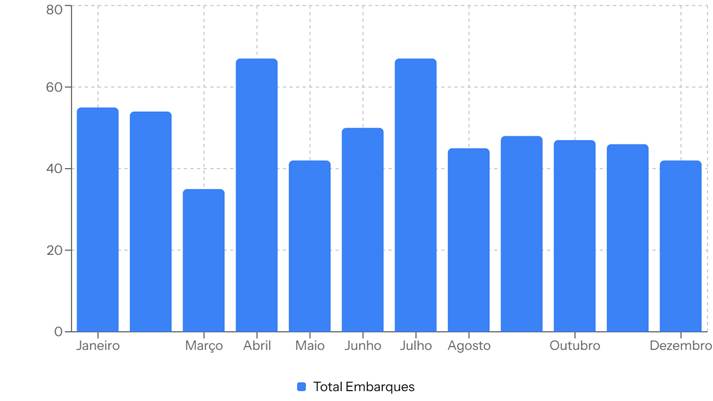
Total de Embarques por mês do ano de 2025 *
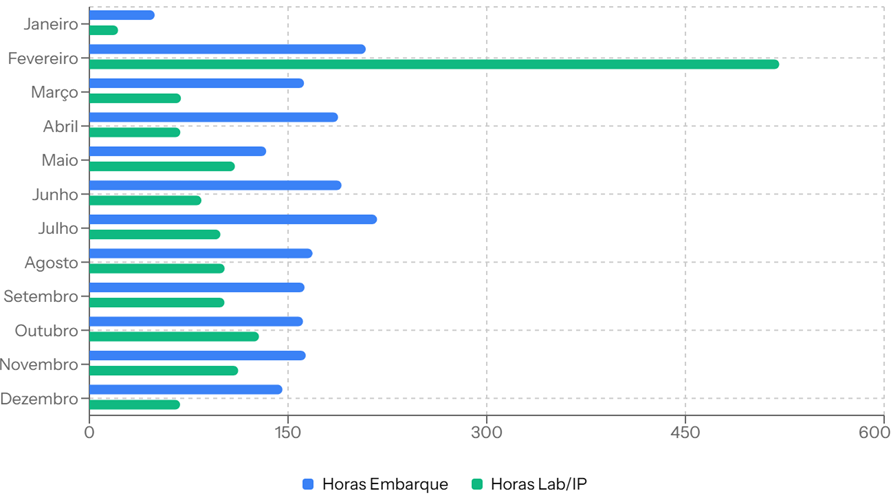
Horas gastas por mês (ano de 2025) com agendamento de embarques , coleta , manipulação e atividades relacionadas a coletas de laboratórios centrais. *
Conclusão
O compliance dos laboratórios centrais não é apenas uma exigência regulatória, mas um compromisso ético com a segurança dos participantes e a integridade científica dos estudos clínicos. Atrasos ou falhas na manipulação de amostras comprometem diretamente esses princípios e devem ser prevenidos por meio de processos robustos, monitoramento contínuo e responsabilidade compartilhada entre patrocinadores, centros de pesquisa e laboratórios.
É urgente a continuidade e aprofundamento das discussões para a implementação de laboratórios centrais no Brasil, minimizando os riscos, custos, e fomentando o ecossistema nacional.
Orientamos que todos os centros de pesquisa clínica fomentem essa discussão junto aos times dos parceiros Patrocinadores. Ainda, indicamos a necessidade dos demais agentes como CROS e Patrocinadores entenderem as limitações da estratégia de utilização de laboratórios centrais fora do país ou America Latina.
Diretoria ACESSE
30 de Março de 2026




